Evropská agentura pro léčivé přípravky (EMA) zahájila přehodnocení vakcín proti HPV virům za účelem podrobnějšího posouzení jejich bezpečnostního profilu. Informuje o tom Státní ústav pro kontrolu léčiv (SÚKL), jehož zprávu publikujeme v kompletním znění:
HPV vakcíny – hodnocení bezpečnostního profilu
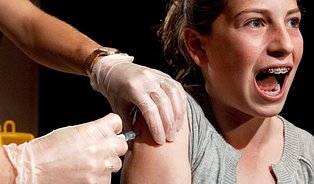
Vakcíny proti lidským papilomavirům (HPV virům) chrání před karcinomem děložního hrdla a různými dalšími typy nádorů a jinými potížemi způsobenými některými sérotypy HPV virů. Karcinom děložního hrdla je čtvrtou nejčastější příčinou úmrtí na zhoubná onemocnění u žen na celém světě. Přestože v Evropě probíhají screeningové programy k včasné detekci rakoviny děložního hrdla, umírají zde na toto onemocnění každoročně desítky tisíc žen. Přínosy vakcín proti HPV virům převyšují možné riziko nežádoucích účinků, což nezpochybňuje ani současné přehodnocení bezpečnosti.
Stejně jako u všech léčivých přípravků, i u těchto vakcín Výbor pro posuzování rizik léčivých přípravků (PRAC) Evropské lékové agentury trvale sleduje a hodnotí veškeré dostupné údaje o bezpečnosti. Současné přehodnocení se týká především dvou typů vzácných nežádoucích účinků – komplexní regionální bolestivý syndrom (CRPS, projevuje se jako chronická bolest končetin) a syndrom posturální ortostatické tachykardie (POTS, abnormální zvýšení srdeční frekvence po posazení se nebo po postavení se, což vyvolává potíže jako je pocit na omdlení, motání hlavy, bolest hlavy, bolest na hrudi a slabost).
Výbor PRAC již dříve hodnotil hlášení těchto nežádoucích účinků u mladých žen po očkování HPV vakcínou, ale nebyla nalezena kauzální souvislost s očkováním. Oba typy potíží se objevují i u neočkovaných, zatím nebylo zjištěno, zda se tyto potíže vyskytují po očkování častěji než v běžné populaci. Dosud bylo celosvětově očkováno přibližně 72 milionů osob HPV vakcínami, v databázích nežádoucích účinků je v současné době 95 případů CRPS a 66 případů POTS.
Cílem současného přehodnocení je ověření frekvence výskytu CRPS a POTS po očkování HPV vakcínami a zjištění, zda mají tyto reakce kauzální souvislost s vakcínami. Podle závěrů hodnocení výbor PRAC rozhodne, zda jsou zapotřebí změny textů informací doprovázejících tyto vakcíny, aby byli lékaři i pacienti adekvátně informováni. Po dobu přehodnocování mají být HPV vakcíny používány stejným způsobem jako dosud.
Více o vakcínách proti lidskému papilomaviru (HPV viru)
V Evropské unii jsou vakcíny proti lidskému papilomaviru dostupné pod názvy: Silgard (Gardasil), Gardasil 9 a Cervarix.
Silgard/Gardasil (registrovaný v září 2006) je určen pro užití u žen i mužů jako prevence premaligních genitálních lézí (cervikálních, vulválních a vaginálních), premaligních análních lézí, cervikálních karcinomů a análních karcinomů v příčinné souvislosti s jistými onkogenními typy lidského papilomaviru (HPV). Dále je určen k prevenci bradavic genitálu (condyloma acuminata) v příčinné souvislosti se specifickými typy HPV.
Přípravek Silgard chrání proti čtyřem typům HPV (typ 6, 11, 16 a 18). Gardasil 9 (registrovaný v červnu 2015) chrání proti devíti typům HPV (typ 6, 11, 16, 18, 31, 33, 45, 52 a 58). Cervarix byl registrován v září 2007 a je určen pro užití u žen a dívek k prevenci premaligních genitálních lézí (cervikálních, vulválních a vaginálních) a cervikálního karcinomu, které jsou způsobeny onkogenními typy lidských papilomavirů 16 a 18.
V současné době jsou v ČR dostupné vakcíny Silgard a Cervarix.